[의약뉴스 in 싱가포르] 한미약품이 개발해 스펙트럼에 라이센스 아웃한 범(凡) HER 표적치료제 포지오티닙이 이전에 최소 두 차례 이상 전신치료경험이 있는 HER2 엑손20 삽입 돌연변이 환자에서 긍정적인 결과를 유지했다.
스펙트럼은 지난 2021년 말 미국에서 비소세포폐암 치료제로 포지오티닙에 대한 시판허가를 신청한 바 있다.
그러나 지난해 미국식품의약국(FDA)는 당시까지의 자료상 환자에게 주는 혜택이 위험보다 크지 않다는 자문위의 권고에 따라 시판허가를 불허했다.
이 가운데 11일, 세계폐암학회 연례학술회의(WCLC 2023)에서는 HER2 양성 비소세포폐암 2차 치료제로 자리를 잡은 다이이찌산쿄의 항체약물접합체(Antibody-Drug Conjugates, ADC) 엔허투(성분명 트라스투주맙데룩스테칸) 등 이전에 최소 두 차례 이상 전신치료를 받은 이력이 있는 난치성 환자들을 대상으로 포지오티닙의 안전성과 효능을 평가한 임상 2상 결과가 발표됐다.
연구에는 총 69명의 환자가 참여했으며, 이전 전신 치료 이력은 2~9회로, 40%는 2회, 51%는 3회 이상 치료 이력이 있었다.
백금기반 요법에 더해 면역항암제를 투약했던 환자가 78%, HER2 항체나 항쳉약물접합체를 투약했던 환자가 36%, 표적치료제를 투약했던 환자는 17%였으며, VEGF 억제제 등 다른 전신요법을 받은 환자가 16%였다.
가장 흔하게 보고된 3등급 이상의 이상반응은 발진(46%), 설사(28%), 점막염(23%) 등이었으며, 치료와 관련해 83%는 용량 중단, 72%는 용량 감소, 13%는 치료를 중단했다.
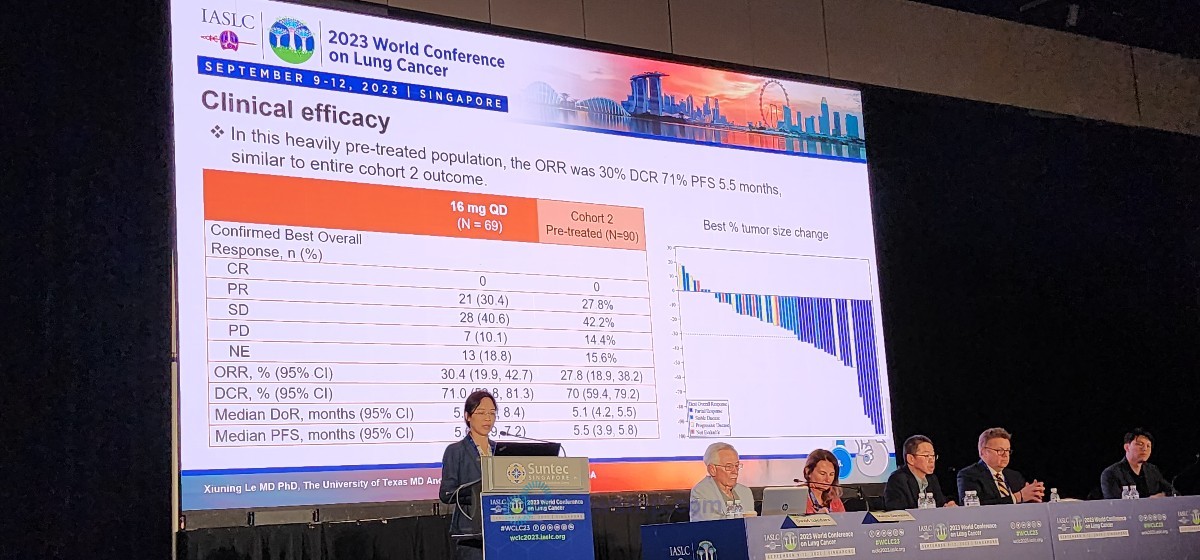
독립적 검토위원회가 평가한 객관적반응률(Objective Response Rate,OR ORR)은 30%(95% CI 19.9~42.7)로, 반응지속기간(Duration of Response, DoR) 중앙값은 5.5개월, 무진행생존기간(Progression-Free Survival, PFS) 중앙값은 5.6개월이었다.
효능은 이전 치료 요법에 상관없이 일관된 경향을 보였으며, 구체적으로 백금이 포함된 모든 전신 요법제가 31.3%, 백금과 도세탁셀 병용요법은 30.8%, 백금과 HER2 항체기반 요법의 병용요법은 24.0%, 백금과 표적치료제 병용요법은 54.5%로 보고됐다.
이와 관련, 연구진은 포지오티닙이 이전에 2차례 이상 전신 치료를 받고 질병이 진행된 HER2엑손20 삽입변이 비소세포폐암 환자에서 임상적으로 의미있는 효능을 입증했다고 평가했다.
특히 연구진은 이 연구가 치료 옵션이 매우 제한적인 HER2 엑손20 삽입변이 비소세포폐암 환자의 3차 이상 치료에서 대규모 데이터셋을 제공하며, 안전성에 있어 새로운 신호는 감지되지 않았다고 전했다.


