[의약뉴스] 아스트라제네카와 다이이찌산쿄의 TROP2 표적 항체약물접합체(ADC) 다트로웨이(성분명 다토포타맙 데룩스테칸)가 요로상피암에서도 긍정적인 결과를 이어가고 있다.
14일(현지시간) 미국임상종양학회 비뇨생식기암 심포지엄(ASCO GU 2025)에서는 다양한 고형종암 환자를 대상으로 진행하고 있는 TROPION-PanTumor01 임상 1상 중 이전에 면역항암제를 포함, 한 차례 이상의 전신 치료 이력이 있는 국소 진행성 또는 전이성 3/4기 요로상피암 환자에 대한 분석 결과가 공개됐다.
중앙 추적 관찰 기간은 10.0개월로, 40명의 환자가 다트로웨이를 투약했으며, 8명이 치료를 유지하고 있었다.
40명의 환자 가운데 24명(60%)이 국소 진행 또는 전이 단계에서 3차례 이상의 치료 이력이 있었고, 36명(90%)는 백금기반 항암화학요법을 받은 이력이 있었으며, 33명(83%)는 파드셉(성분명 엔포투맙베도틴, 아스텔라스)을 투약했다.
다만, 이전에 TROP2 표적 항체약물접합체 투약 이력이 있는 환자는 연구에 참여할 수 없었다.
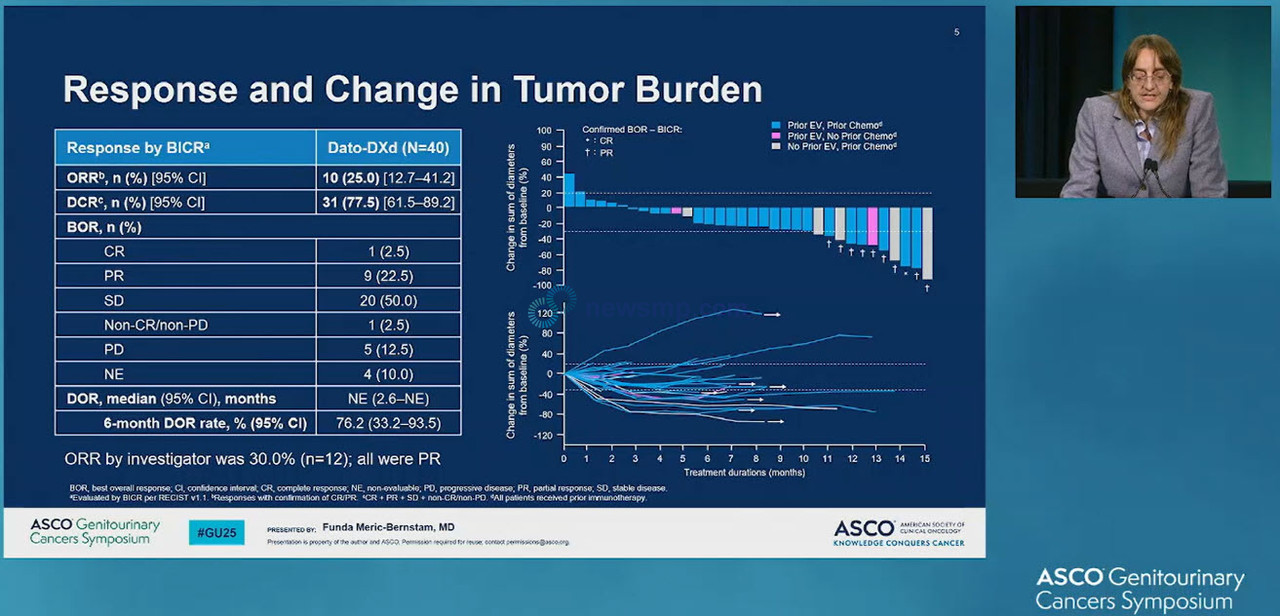
분석 결과, 연구진이 평가한 객관적 반응률(Objective Response Rate, ORR)은 30.0%로 모두 부분반응(Partial Response, PR)이었으며, 독립적 검토위원회가 평가한 객관적 반응률은 1명의 완전반응(Complete Response, CR)을 포함, 25.0%로 보고됐다.
중앙 추적관찰 기간까지 반응 지속기간(Duration of Reponse, DoR)은 중앙값에 이르지 않았으며, 반응이 나타난 환자의 76.2%가 6개월까지 반응을 유지했다.
독립적 검토위원회가 평가한 무진행생존기간(Progression-Free Survival, PFS) 중앙값은 6.9개월로 집계됐다.
치료와 관련한 3등급 이상의 이상반응은 55%에서 보고됐으며, 심각한 이상반응이나 4~5등급 이상반응은 보고되지 않았다.
치료와 관련한 이상반응으로 인한 치료 중단, 용량 감량, 일시 중단은 각각 8%와 20%, 35%에서 발생했다. 또한 2명의 환자에서 약물과 관련한 2~3등급 간질성 폐렴이 보고됐다.
이와 관련, 연구진은 이전 치료 이력이 많은 국소 진행성 또는 전이성 요로상피암 환자에서 다트로웨이가 관리 가능한 수준의 안전성 프로파일로 고무적인 항종양 활성을 보였다고 평가했다.


