지난 8월 이후 계속해서 증가 추세를 보인 임상시험 승인 건수가 지난 6월 이후 다시 한 번 60건을 넘어서면서 활성화되는 모습을 보였다.
11월 한 달 동안 식품의약품안전처의 승인을 받은 임상시험은 총 61건으로 전월 56건 대비 8.9%, 전년 동월 54건 대비 13.0% 증가한 것으로 나타났다.
6월 이후 월별 임상시험 승인 건수를 살펴보면 6월 61건으로 정점을 찍은 뒤 8월에 45건까지 줄었지만, 이후 9월 50건, 10월 56건으로 늘어난데 이어 11월에 다시 한 번 연중 최고치를 기록한 것이다.
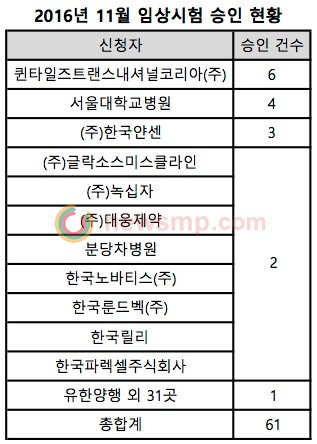
신청자별로 살펴보면 퀸타일즈트랜스내셔널코리아가 6건으로 가장 많았으며, 서울대학교병원이 4건, 한국얀센 3건, 녹십자와 대웅제약, GSK, 분당차병원, 한국노바티스, 한국룬드벡, 한국릴리, 한국파렉셀이 각 2건씩 승인 받았고, 유한양행을 비롯한 총 32곳에서 각 1건씩의 임상시험을 승인 받았다.
국내 주요 제약사의 임상시험 현황을 살펴보면 녹십자가 헌터증후군 치료제인 헌터라제의 임상3상시험과 혈우병치료제 그린진에프주2000단위의 임상2상시험을 승인받았다.
대웅제약은 항궤양제 개량신약인 DWJ1366의 임상1상시험과 DWJ1392의 임상1상시험을 승인 받았고, 일동제약은 놀텍정을 아목시실린, 클래리스로마이신과 병용 투여하는 임상1상시험을, 동아에스티는 타리온정의 서방형 제제인 DA-5206의 임상1상을, 유한양행은 리리카 개량신약인 YHD1119의 임상3상 시험을, 보령제약은 카나브와 리피토 복합제에 대한 임상1상 시험을 각각 승인 받았다.
한편 임상시험 단계별로는 임상3상이 17건으로 가장 많았으며, 1상 14건, 연구자임상 10건, 2상 8건, 1/2상 4건, 1/3상과 2b/3상, 2b상이 각 2건, 2/3상과 2a상이 각 1건씩이었다.


