MSD의 면역항암제 키트루다(성분명 펨브롤리주맙)가 아시아의 PD-L1 음성 비소세포폐암 환자에서 가치를 재확인했다.
8일(현지시간) 개막한 유럽임상종양학회 면역항암 학술대회(ESMO Immuno-oncology Congress 2021, ESMO IO)에서는 일본과 중국, 대만의 연구진이 KEYNOTE-021 cohort G, KEYNOTE-189 및 KEYNOTE-189 일본 확장 연구, KEYNOTE-407 및 KEYNOTE-407 중국 확장 연구 등 5가지 연구를 통합 분석한 결과를 포스터를 통해 발표했다.

이 연구들은 이전 전신치료 경험이 없는 진행성 비소세포폐암 환자들을 대상으로 키트루다와 항암화학 병용요법의 안전성과 유효성을 항암화학 단독요법과 비교했다.
앞서 지난 2019년에는 세계폐암학회(IASLC 2019 World Conference)에서 KEYNOTE-021, KEYNOTE-189, KEYNOTE-407 등 3개 연구 중 PD-L1 음성(TPS<1)인 환자에 대한 통합 분석결과가 공개된 바 있다.
당시 연구진은 키트루다+항암화학 병용요법이 항암화학 단독요법에 비해 전체생존율(Overall Survival, OS)은 물론 무진행생존율(Progression-Free Survival, PFS), 2차 무진행생존율, 객관적반응률(Objective Rresponse Rate, ORR)까지 개선했다고 발표했다.
이번에 ESMO IO를 통해 공개된 통합분석은 이 3가지 연구에 일본, 중국 확장 연구를 포함, 총 5가지 연구 중 PD-L1 음성인 동아시아인 환자들을 추려내 안전성과 유효성을 평가했다.
통합 분석의 중앙 추적관찰 기간은 무작위 배정 후 33.4개월로, 5가지 연구에 참여한 총 1438명의 환자 중 PD-L1 음성 동아시아인 107명(7.4%)을 대상으로 진행됐다.
데이터 수집 마감(cut-off) 시점에 키트루다 병용요법군의 환자 중 9명, 항암화학요법군 중 1명이 사전에 설정했던 치료 스케줄을 완료했으며, 각 그룹에서 1명의 환자가 치료를 진행하고 있었다.
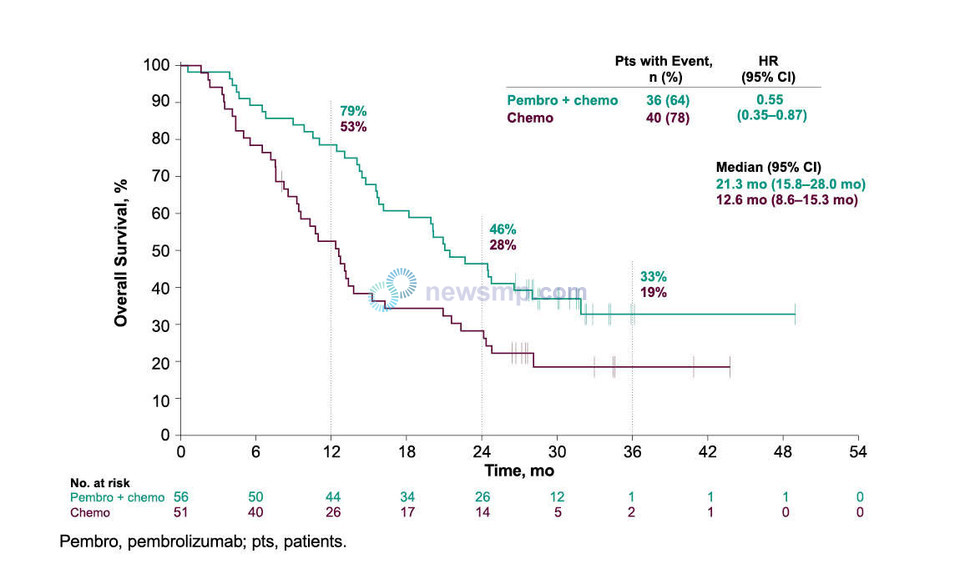
분석 결과 전체생존기간 중앙값은 키트루다 병용요법군이 21.3개월로 항암화학 단독요법군의 12.6개월의 두 배에 가까웠으며, 사망의 위험은 45%(HR=0.55)를 줄인 것으로 집계됐다.
이는 앞서 2019년 발표된 3개 연구의 통합분석과 거의 비슷한 수치로, 당시 키트루다 병용요법군의 사망위험은 항암화학요법군보다 44% 더 낮았던 것으로 집계된 바 있다.
전체생존율은 12개월 시점에 키트루다 병용요법군이 79%, 항암화학 단독요법군은 53%로 집계돼 양군 모두 2019년 발표된 연구 결과보다 상대적으로 더 높았다.
당시 12개월 시점의 추정 전체 생존율은 키트루다 병용요법군이 66%, 항암화학요법군은 47%로 집계됐다.
이번 연구에서 전체생존율의 차이는 12개월 이후에도 지속적으로 유지, 24개월 시점에는 46%와 28%로 집계됐고, 36개월 시점에는 33%와 19%로 추정됐다.
무진행생존기간 중앙값은 키트루다병용요법군이 8.4개월, 항암화학 단독요법은 6.0개월로, 키트루다군의 질병 진행 또는 사망의 위험 36% 더 낮았다.(HR=0.64) 이 역시 지난 2019년에 발표됐던 상대위험비(HR=0.67)와 비슷한 수치다.
12개월 시점의 무진행 생존율은 키트루다군이 33%, 항암화학 단독요법군은 17%로 두 배에 가까운 차이를 보였으며, 24개월 시점에는 17%와 10%로 집계됐다.
1차 치료가 후속 치료에 미치는 영향을 보여주는 2차 무진행 생존기간도 키트루다 병용요법군의 중앙값이 15.8개월로 항암화학 단독요법군의 9.0개월을 크게 상회, 2차 질병 진행 또는 사망의 위험을 57%(HR=0.43) 줄인 것으로 집계됐다.
12개월 시점의 2차 무진행 생존율은 키트루다 병용요법이 68%, 항암화학 단독요법군은 27%로 두 배 이상 차이를 보였고, 24개월 시점에도 34%와 15%로 차이를 유지했다.
종양 반응에 있어서는 키트루다 병용요법군의 객관적 반응률이 1명의 완전반응(Complete Response, CR)을 포함, 71.4%로 항암화학 단독요법군의 43.1%보다 30%p 가까이 높았다.
반응지속기간(Duration of Response, DOR) 중앙값도 키트루다 병용요법이 6.7개월로 항암화학 단독요법의 4.9개월보다 2개월 가까이 더 길었다.
안전성에 있어 3~5등급 이상반응 발현율은 큰 차이가 없었으나, 치료 중단으로 이어진 이상반응은 키트루다 병용요법군이 21.4%로 11.8%의 항암화학 단독요법보다 두 배 이상 높았고, 사망으로 이어진 환자는 키트루다군이 56명 중 3명, 항암화학요법에서는 51명 중 2명으로 집계됐다.
한편, 키트루다 병용요법군에서 35차례의 투약 스케줄을 모두 마무리한 9명의 환자는 모두 부분 반응(Partial Response, PR)을 보였으며, 반응지속기간 중앙값은 31.1개월에 달했고, 모두 자료 수집 마감때까지 생존해 있었다.
또한 항암화학 단독요법군의 환자 가운데 18명이 키트루다 단독요법으로 후속치료를 받았으며, 이들의 키트루다 투약 후 전체 생존기간 중앙값은 11.7개월, 30개월 시점 추정 전체생존율은 25.0%로 집계됐다.


