국내 제약사들이 미국 시장 진출을 위해 다각적인 전략을 펼치는 가운데 미국 FDA의 임상 및 시판 승인 성공률에도 관심이 모아지고 있다.
SK증권은 29일 보고서를 통해 FDA의 임상 단계별 및 분야별 성공률을 조사한 결과를 공개했다.
보고서에 따르면 2006년부터 2015년까지 10년간 FDA에서 임상을 수행했거나 진행 중인 자료를 조사한 결과 모든 임상들에 대해 임상1상부터 신약승인까지 성공률은 평균 9.6%로 조사됐다.
단계별로는 임상1상 통과 가능성이 63.2%였으며, 임상2상은 30.7%, 임상3상은 58.1%였으며, 신약 승인 단계인 NDA(New Drug Application)/BLA(Biologic License Application)는 85.3%로 가장 높았다.
보고서의 설명에 따르면 임상1상은 주로 정상인을 대상으로 약물의 독성테스트를 하는 과정으로, 약물의 효과는 평가하지 않고 안전성에 초점을 맞추기 때문에 대부분 성공률이 높다.
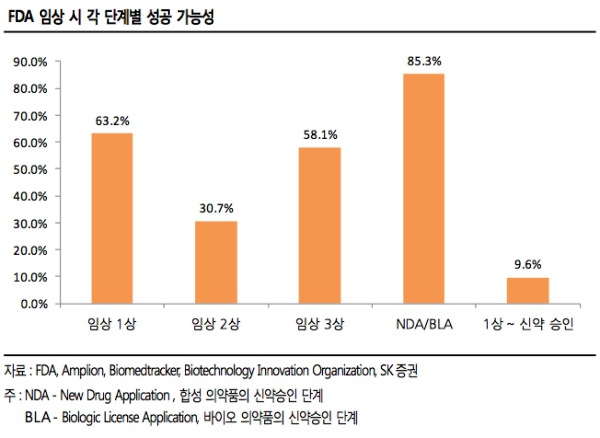
그러나 임상2상은 인체(환자)를 대상으로 부작용뿐 아니라 약효를 테스트하는 첫 번째 관문이기 때문에 성공률이 제일 낮을 수밖에 없다.
임상3상은 임상2상과 같이 환자를 대상으로 약효와 부작용을 보는 단계지만, 환자 수가 많고 약의 투여 용량을 결정하게 된다는 차이가 있다. 이미 임상2상에서 약효와 부작용을 테스트했기 때문에 비교적 성공 확률이 높다.
NDA 및 BLA 단계에서는 임상1상에서 3상까지 해당 적응증에 대한 모든 임상시험을 통과한 상태에서 다시 한 번 최종 검토하는 과정이기 때문에 사실상 통과할 확률이 높다.
한편 희귀성 질환의 경우 평균 성공률 9.6%보다 3배 가까이 높은 25.3%의 성공률을 기록한 반면 항암제는 5.1%로 평균의 절반 수준에 불과했다.
합성의약품(NME)과 바이오의약품, Non-NME(신약 승인된 약물의 복합체 또는 개량신약)를 비교해보면, 임상1상에서 신약 승인까지 Non-NME의 성공률이 22.6%로 가장 높았고, 바이오의약품이 11.5%, 합성의약품 6.2% 순이었다.
보고서는 이에 대해 Non-NME가 기존 승인된 신약을 바탕으로 임상시험을 진행하는 만큼 승인률이 높았고, 바이오의약품의 경우 일반적으로 합성의약품 대비 약효가 높고 부작용이 적어 성공률이 상대적으로 높다고 설명했다.


