[의약뉴스] 옵디보(성분명 니볼루맙, BMSㆍ오노)와 카보메틱스(성분명 카보잔티닙, 입센)가 진행성/전이성 신장암(신세포암)의 표준요법으로서 철옹성을 쌓아가고 있다.
15일(현지시간) 미국임상종양학회 비뇨생식기암 심포지엄(ASCO 2025)에서는 신세포암 환자에서 옵디보와 카보메틱스 조합을 평가한 두 건의 3상 임상, CheckMate 9ER와 COSMIC-313의 추가 관찰 결과가 공개됐다.
이 가운데 CheckMate 9ER은 이전 치료 이력이 없는 신세포암 환자 651명을 대상으로 옵디보와 카보메틱스 병용요법을 수텐(성분명 수니티닙, 화이자)와 비교하고 있는 3상 임상이다.
앞서 3년차 분석까지 옵디보와 카보메틱스 병용요법은 무진행생존율(Progression-Free Survival, PFS)과 전체생존율(Overall Survival, OS), 객관적반응률(Objective Response Rate, ORR) 등에서 수텐 단독요법 대비 유의미한 이득이 있는 것으로 확인됐다.
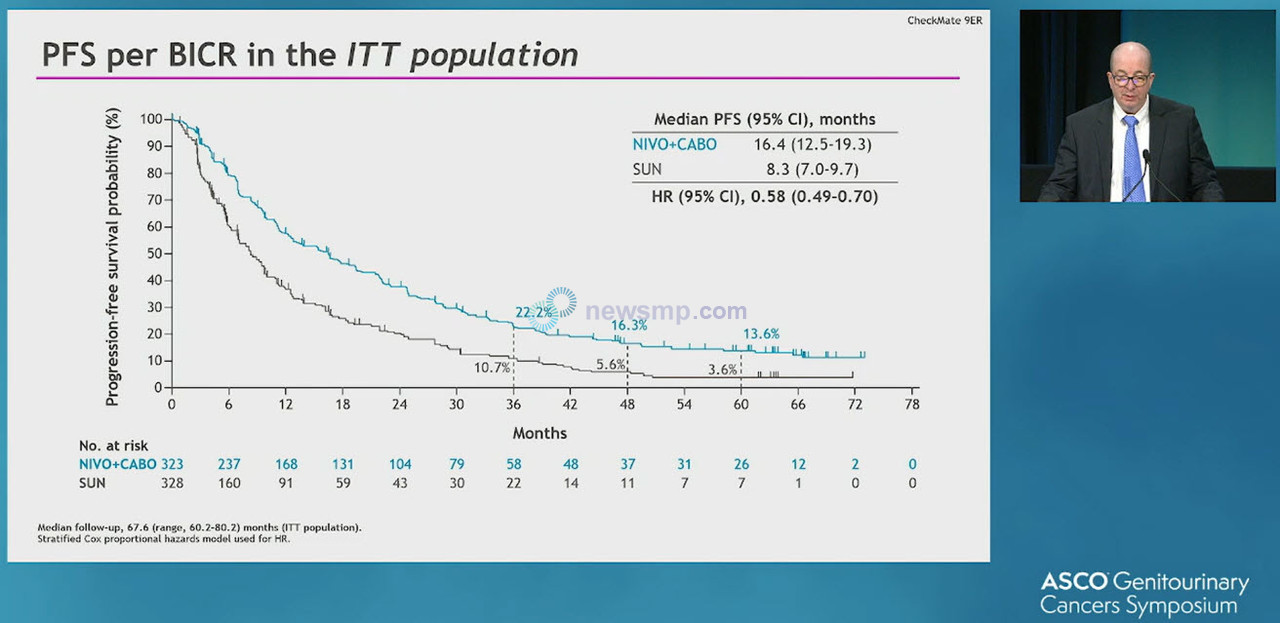
15일 발표된 최종 추적 관찰 결과는 5년차(중앙 추적관찰 67.6개월) 분석으로, 옵디보와 카보메틱스 병용요법의 장기적인 효능을 확인했다는 것이 연구진의 설명이다.
전체 환자군에서 무진행생존기간 중앙값은 옵디보와 카보메틱스 병용요법이 16.4개월, 수텐 단독요법군은 8.3개월, 60개월 무진행생존율은 13.6%와 3.6%로 옵디보+카보메틱스 병용요법군의 질병 진행 또는 사망의 위험이 42% 더 낮았다(HR=58, 95% CI 0.49-0.70).
전체생존기간 중앙값 또한 옵디보와 카보메틱스 병용요법군이 46.5개월, 수텐 단독요법군은 35.5개월, 60개월 전체생존율은 40.9%와 35.4%로 옵디보+카보메틱스 병용요법군의 사망 위험이 21% 더 낮았다(HR=0.79, 95% CI 0.65-0.96).
객관적 반응률 또한 옵디보와 카보메틱스 병용요법군이 13.9%의 완전반응(Complete Respoinse, CR)을 포함, 55.7%로 수텐군의 27.4%(완전반응 4.6%)를 크게 상회했다.
반응지속기간(Duration of Response, DoR) 중앙값 또한 옵디보와 카보메틱스 병용요법군이 22.0개월로 수텐군의 15.2개월을 상회했으며, 60개월 반응 지속률 또한 22.0%와 10.0%로 옵디보+카보메틱스군이 수텐군을 웃돌았다.
다만, 3년차 분석과 마찬가지로 IMDC(International Metastatic RCC Database Consortium, 국제 전이성 신세포암 데이터베이스 컨소시엄) 위험도 분류 기준 저위험군(Favorable risk)에서는 옵디보와 카보메틱스 병용요법군의 전체생존 이득은 뚜렷하지 않았다.
저위험군에서 전체생존기간 중앙값이 옵디보와 카보메틱스 병용요법군이 53.7개월로 수텐군의 58.9개월을 하회했고, 60개월 전체생존율 또한 옵디보+카보메틱스 병용요법군이 46.3%로 수텐군의 49.4%를 밑돈 것.(HR=1.08, 95% CI 0.70-1.66)
그러나 무진행 생존기간 중앙값은 저위험군에서도 각각 21.4개월과 12.8개월로 옵디보와 카보메틱스군이 수텐군을 상회했으며, 60개월 무진행생존율도 15.1%와 3.9%로 상당한 차이를 보였다.(HR=0.67 95% CI 0.46-0.97)
객관적 반응률은 66.2%와 43.1%, 완전반응률은 16.2%와 6.9%로 옵디보와 카보메틱스 병용요법군이 수텐군을 상회했다.
중간위험군(Intermediate risk)에서 무진행생존기간 중앙값은 16.6개월과 8.5개월, 60개월 무진행생존율은 12.7%와 4.7%(HR=0.63, 95% CI 0.50-0.80), 전체생존기간 중앙값은 47.4개월과 36.2개월, 60개월 전체생존율은 41.2%와 38.2%(HR=0.86, 95% CI 0.67-1.11)로 모두 옵디보와 카보메틱스 병용군이 수텐군을 웃돌았다.
객관적반응률은 55.9%와 27.7%, 완전반응률은 15.4%와 4.8%, 60개월 반응 지속률은 19.0%와 13.0%로 역시 옵디보와 카보메틱스 병용군이 수텐군을 상회했다.
고위험군(Poor risk)군에서 무진행생존기간 중앙값은 9.9개월과 4.2개월, 60개월 무진행생존율은 15.7%와 0%(HR=0.36, 95% CI 0.23-0.56), 전체생존기간 중앙값은 34.8개월과 10.5개월, 60개월 전체생존율은 33.1%와 12.9%(HR=0.49, 95% CI 0.33-0.74)로 더욱 뚜렷한 차이를 보였다.
객관적반응률은 42.6%와 10.3%, 완전반응률은 6.6%와 1.5%, 60개월 반응 지속률은 37.0%와 0.0%로 상당한 차이를 보였다.
간과 뼈, 폐 등 기저시점의 전위 위치에 따른 차이는 없었다. 간전이 환자에서 무진행생존기간 중앙값은 두 그룹이 각각 10.9개월과 6.2개월(HR=0.55, 95% CI 0.37-0.82), 전체생존기간 중앙값은 37.6개월과 22.1개월(HR=0.65, 95% CI 41-0.97), 객관적 반응률은 52.1%와 21.4%로 집계됐다.
뼈 전이 환자에서도 무진행생존기간 중앙값은 13.8개월과 5.3개월(HR=0.43, 95% CI 0.30-0.64), 전체생존기간 중앙값은 34.8개월과 20.7개월(HR=0.66, 95% CI 0.45-0.95), 객관적 반응률은 49.4%와 9.3%로 모두 옵디보와 카보메틱스 병용요법군이 수텐군을 크게 상회했다.
폐 전이 환자 역시 무진행생존기간 중앙값이 9.4개월과 8.3개월(HR=0.56, 95% CI 0.46-0.69), 전체생존기간 중앙값은 47.5개월과 37.4개월(HR=0.75, 95% CI 0.60-0.94), 객관적 반응률은 57.3%와 27.9%로 옵디보와 카보메틱스 병용요법군이 수텐군을 웃돌았다.
안전성에 있어서는 이전에 보고된 양상이 유지됐으며, 새로운 이상반응은 신호는 관찰되지 않았다.
이와 관련, 연구진은 최종 추적 관찰에서 수텐 대비 옵디보와 카보메틱스 병용요법의 장기 이득을 확인했으며, 이는 이 조합을 진행성 신세포암 1차 치료의 표준 요법으로서 지속적으로 지지하는 결과라고 의미를 부여했다.
COSMIC-313 3상 역시 이전 치료 이력이 없는 진행성 신세포암 환자 총 855명을 모집, 옵디보와 여보이(성분명 이필리무맙, BMS), 카보메틱스 3제 요법을 옵디보와 여보이 2제 요법과 비교하고 있다.
앞서 17.7개월차 분석에서는 3제요법군이 무진행생존율과 전체생존율, 객관적반응률이 모두 2제요법군을 상회했으며, 특히 고위험군에 비해 중간위험군에서 더욱 뚜렷한 차이를 보였다.
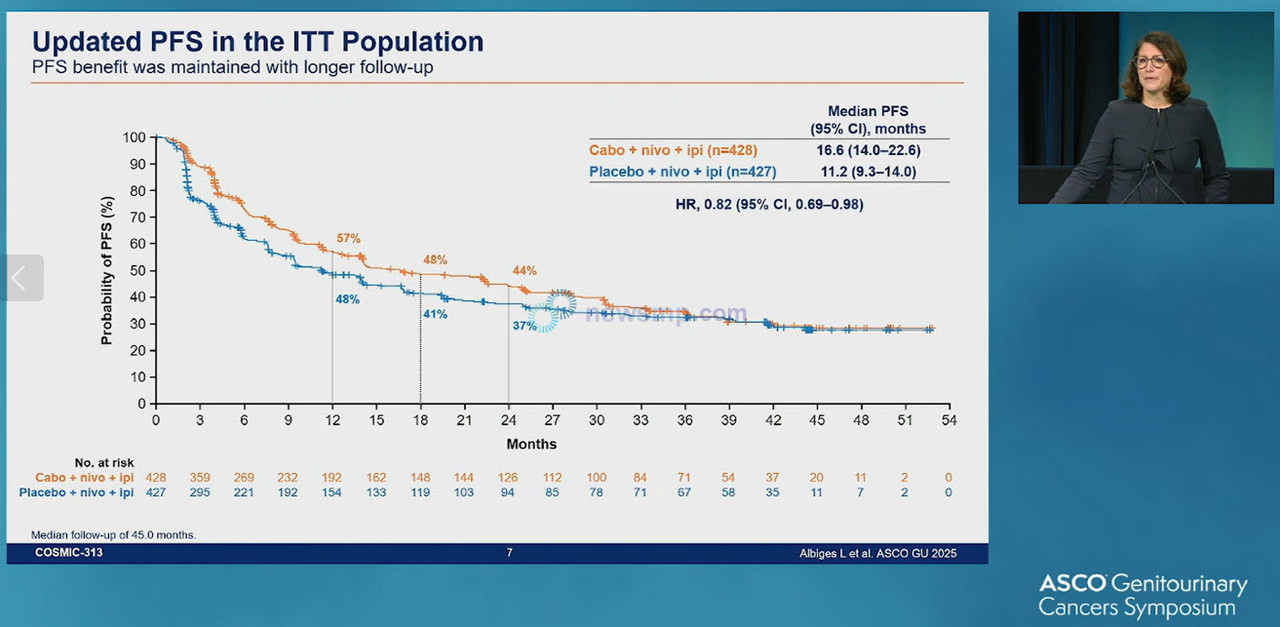
15일 공개된 추가 분석은 중앙 추적관찰 45.0개월 시점의 자료로, 무진행생존율에서는 3제 요법의 이득이 유지됐으나, 전체생존율에서는 의미있는 차이를 보이지 않았다.
다만, 탐색적 분석을 통해 3제 요법을 통해 전체생존율에 이득을 얻을 수 있는 환자군을 찾아냈다.
구체적으로, 무진행생존기간 중앙값은 3제 요법군이 16.6개월로 2제 요법군의 11.2개월을 상회했으나(HR=0.82 95% CI 0.69-0.98), 전체 생존기간 중앙값은 41.9개월과 42.0개월로 차이가 없었다(HR=1.02, 95% CI 0.85-1.23).
객관적반응률은 3제 요법군이 4%의 완전반응을 포함 46%로 3%의 완전반응을 포함 37%의 2제 요법을 상회했다.
또한, 전체생존율은 기저 시점의 c-Met이나 PD-L1 발현율에 상관없이 차이를 보이지 않았다.
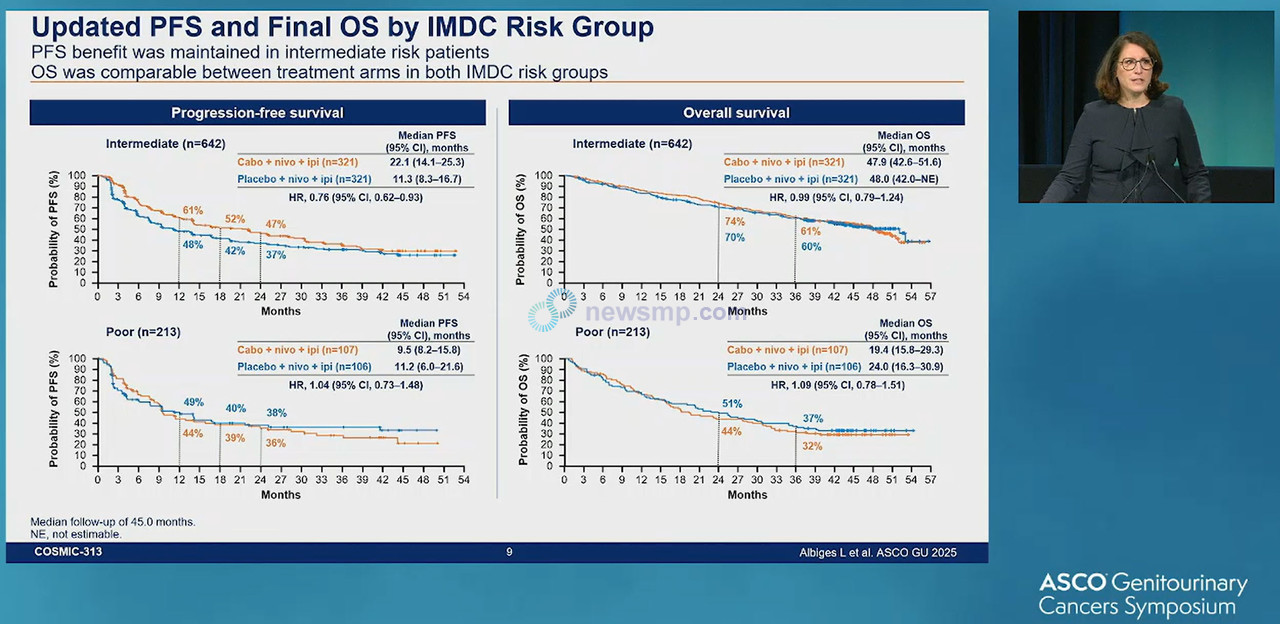
위험도에 따라서는 중간위험군에서 무진행생존기간 중앙값이 22.1개월과 11.3개월(HR=0.76, 95% CI 0.62-0.93)으로 3제 요법군이 2제 요법을 상회했으나, 전체생존기간 중앙값은 47.9개월과 48.0개월(HR=0.99, 95% CI 0.79-1.24)로 차이가 없었다.
나아가 고위험군에서는 무진행생존기간 중앙값이 9.5개월과 11.2개월(HR=1.04, 95% CI 0.73-1.48), 전체생존기간 중앙값은 19.4개월과 24.0개월(HR=1.09 95% CI 0.78-1.51)로 집계돼 수치적으로는 3제 요법군이 더 짧았다.
다만, 탐색적 분석에서 M2 유형의 대식세포가 많을수록 3제 요법의 이득이 더 뚜렷하게 나타났다.
M2 유형 대식세포가 많은 환자에서 무진행생존기간 중앙값은 3제 요법이 10.1개월로 2제 요법의 5.95개월(HR=0.48, 95% CI 0.29-0.81)을 상회했으며, 전체생존기간 중앙값 역시 각각 39.9개월과 23.0개월(HR=0.51, 95% CI 0.31-0.86)로 3제 요법이 2제 요법을 크게 웃돌았다.
M2 유형 대식세포가 적은 환자에서도 수치상으로는 3제 요법의 무진행생존기간 중앙값이 22.1개월로 2제 요법의 16.7개월(HR=0.89, 95% CI 0.66-1.20)보다 길었지만, 전체생존기간은 2제 요법이 중앙값에 이르지 않은 가운데 3제 요법은 47.8개월(HR=1.2, 95% CI 0.88-1.70)에 머물렀다.


