1,374품목, 생동인정 生 - 불인정 死
2,053품목도 문헌재평가 실시
‘생동성 인정을 통해 계속해서 시장에서 살아남느냐, 불인정으로 퇴출되느냐.’
식품의약품안전청은 지난달 31일 ‘2008년도 의약품 재평가 실시’한다는 공고문을 띄웠다.
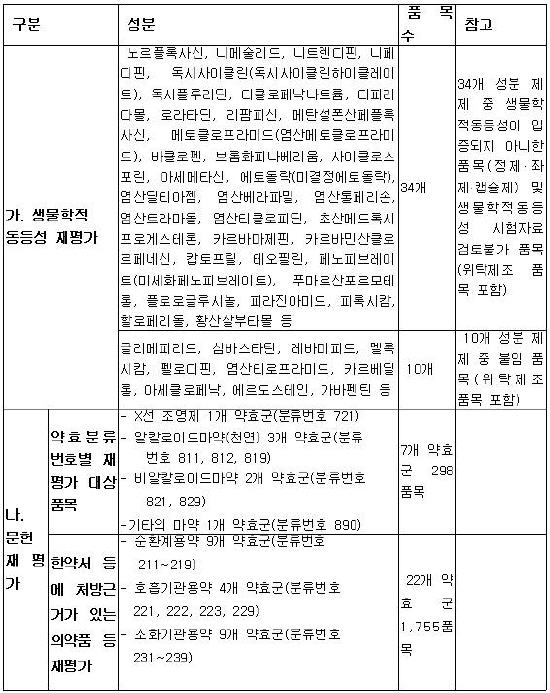
공고문은 크게 ▲생물학적동등성 재평가대상 - 44개 성분(1,374품목) ▲문헌 재평가 대상 - 29개 약효군(2,053품목)이 해당된다고 밝혔다. (구체적인 대상 품목 : 우측 자료실 참고)
이 품목에 해당하는 각 제약업체들은 ‘생물학적동등성시험계획서’는 오는 11월 30일까지, 생물학적동등성시험 결과보고서‘는 내년 5월 31일까지 제출해야 한다.
 | ||
| ▲ 생동인정여부에 따라 시장에서 살아남느냐, 퇴출 되느냐가 결정된다. | ||
식약청 관계자는 3일 전화통화에서 “생동 재평가 품목의 경우 대부분 허가 시 생동 의무화 품목이 아닌 경우가 많았고 또 일부는 지난해 생동성 시험기간에 검토불가 시험자료로 인한 품목도 해당 된다”며 이번 생동성 재평가 이유를 들었다.
이어 이 관계자는 “최종심사는 제반서류를 받은 내년 6월부터 하게 된다”고 전했다.
그는 심사결과와 관련해, “만약 생동성을 입증하지 못하면 시장에서 퇴출된다. 반면 생동성이 인정되면 대체조제가 가능하게 된다”고 설명했다.
아울러 식약청은 문헌 재평가 대상(총 29개 약효군 2,053품목)도 공고했다.
이에 해당되는 제약사들은 품목별로 의약품 재평가 신청서를 작성하여 오는 12월 31일까지 식약청에 제출해야 한다.
식약청 관계자는 “문헌 재평가의 경우 외국 사례, 최신자료 등을 수집해 재평가 한다”고 말했다.
한편, 생동재평가 대상 품목 중 대표품목을 살펴보면 ▲신풍제약 ’가바렙캡슐 300mg ▲한미약품 ‘가바페닌캡슐’ ▲동화약품 ‘가바펙트캡슐 300mg ▲일양약품 ‘글리메드정 2mg' ▲현대약품 ’글리메린정 2mg' ▲드림파마 ‘다마릴정 2mg' ▲중외제약 ’메피그릴정‘ ▲종근당 ‘가바렙정 800mg' ▲진양제약 ’미아릴정‘’ ▲녹십자 ‘아마그린정 2mg' ▲보령제약 ’‘보령글리메피리드정 2mg' ▲대웅제약 ’유글렉스정 2mg' 등으로 나타났다.
문헌 재평가 대상 품목 중 대표품목을 들여다보면 ▲대한약품공업 ‘보노렉스 300주’ ▲게르베코리아 ‘리피오돌울트라액’ ▲일성신약 ‘이오파미로300주사액30ml ▲태준제약 ’엠알베스터주‘ ▲한국쉐링 ’레보비스트주사‘ ▲동국제약 ’파미레이200주사액‘ ▲한국얀센 ’타이레놀위드코데인정30mg' ▲명문제약 ‘스토몰주사1mg'으로 드러났다.