[의약뉴스] 길리어드의 Trop-2 표적 항체약물접합체(Antibody Drug Conjugate, ADC) 트로델비(성분명 사시투주맙 고비테칸)가 면역항암요법에 실패한 전이성 요로상피세포암 환자에서 의미있는 결과를 도출했다.
18일(한국시간) 미국 임상종양학회 비뇨생식기암 심포지엄(ASCO GU 2023)에서는 전이성 요로상피세포암 환자를 대상으로 트로델비의 가능성을 평가하고 있는 TROPHY-U-01 임상 2상 중 코호트2에 대한 1차 분석 결과가 공개됐다.
코호트2는 이전에 면역항암요법을 받았으나 질병이 진행한 전이성 요로상피세포암 환자로 백금 항암화학요법이 불가능한 환자들에서 트로델비 10mg/kg (1일, 8일, 이후 매 21일)의 유효성을 평가하고 있다.
연구의 1차 평가변수는 객관적반응률(Objective Response Rate, ORR), 2차 평가변수는 반응지속기간(Duration of Respnse, DoR), 임상적이득률(Clinical Benefit Rate, CBR), 무진행생존율(Progression-Free Survival, PFS) 등으로 정의했다.
연구에 참여한 38명의 환자 가운데 66%는 원격 전이를 동반하고 있었으며, 전이 부위로는 66%가 내장전이로, 29%는 간전이가 있었다.
이전 항암요법은 중앙값 기준 2차례로, 전체 환자 중 74%가 2차례 이하의 항암요법을 받았었다.
이전 면역항암 요법은 58%다 키트루다(성분명 펨브롤리주맙, MSD), 26%가 티쎈트릭(성분명 아테졸리주맙, 로슈), 13%는 옵디보(성분명 니볼루맙, BMSㆍ오노), 그 외 임핀지(성분명 더발루맙, 아스트라제네카)와 여보이(성분명 이필리무맙, BMS)가 각각 3%로 집계됐다.
절반의 환자들은 이전에 수술 보조요법으로 백금치료를 받았으며, 18%는 파드세브(성분명 엔포투맙 베토딘, 아스텔라스) 치료 이력이 있었다.
이전 전신 치료에서는 완전반응(Complete Response, CR)이 있었던 환자가 1명(3%), 부분반응(Partial Response, PR)이 있었던 환자가 6명(16%), 안정병변(Stable Disease, SD)의 환자가 13명(34%)이었으며 질병 진행(Progressive Disease, PD)은 22명(58%)으로 절반을 넘었다.
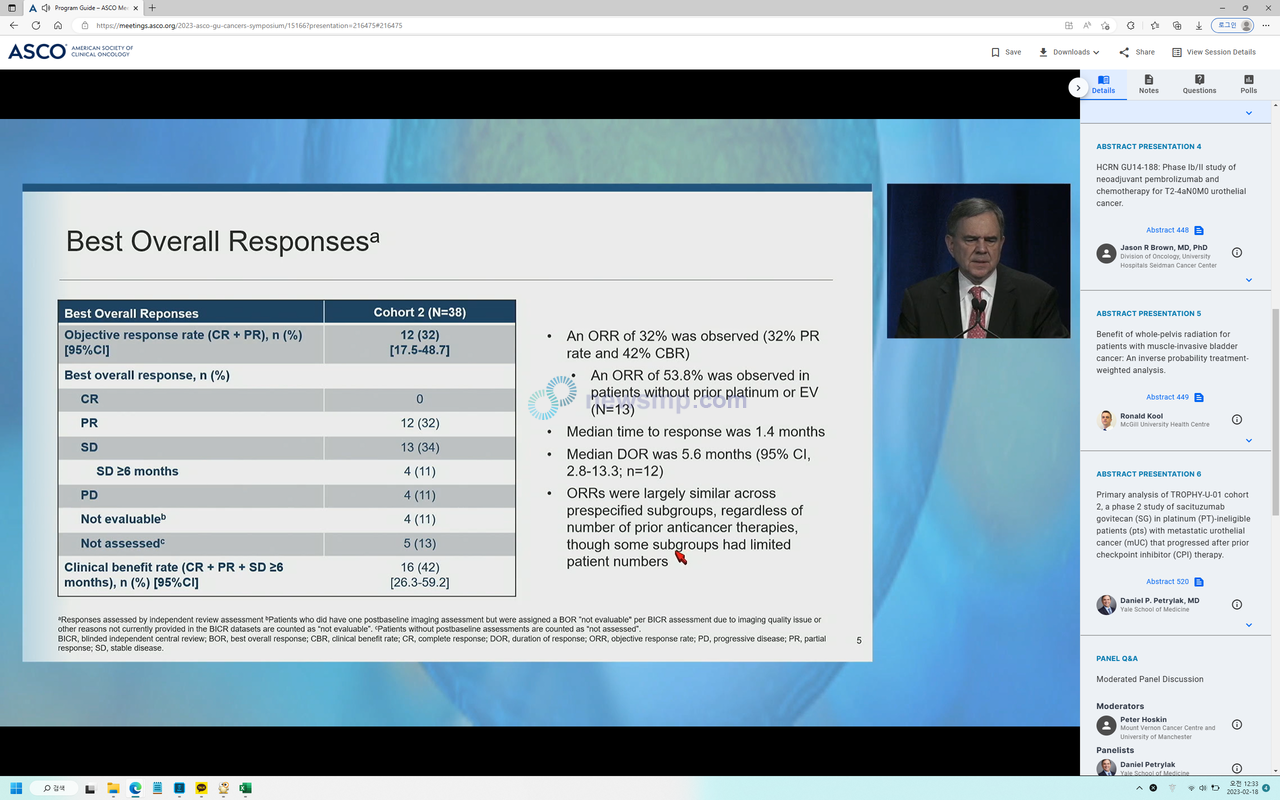
1차 분석 결과 트로델비의 객관적반응률은 32%(12명)로 모두 부분반응이었으며, 안정병변이 34%(13명)로 6개월 이상 유지된 환자가 11%(4명)이었다.
임상적 이득률(완전반응+부분반응+6개월 이상 안정병변)은 42%(15명)으로 집계됐다.
반응이 나타나기까지의 시간(Time To Response, TTR) 중앙값은 1.4개월, 반응 지속기간 중앙값은 5.6개월로 집계됐다.
이 가운데 이전에 백금이나 파드세브 치료 이력이 없는 환자에서는 객관적반응률이 52.8%로 더 높았다.
전체 환자들을 치료 시작시점부터 질병이 진행하기까지 분석한 결과 69%의 환자에서 병변의 크기가 줄어들었던 것으로 확인됐다.
이외에 무진행생존기간 중앙값은 5.6개월, 전체생존기간 중앙값은 13.5개월로 집계됐다.
안전성에 있어서는 68%의 환자에서 치료와 관련한 3등급 이상의 이상반응이 보고됐으며, 가장 흔한 이상반응은 호중구감소증(34%), 빈혈(21%), 백혈구감소증(18%), 피로(18%), 설사(16%) 등이었다.
3명(8%)의 환자에서 치료와 관련한 열성 호중구 감소증이 보고됐으며, 이 가운데 2명은 3등급, 1명은 4등급이었다.
14명(37%)의 환자가 치료 관련 이상반으로 트로델비 투여량을 감량했으며, 7명(18%)는 치료 관련 이상반응으로 치료를 중단했으나, 치료 관련 이상반응으로 인한 사망은 없었다.
결과적으로 이상반응은 관리가 가능한 수준이었으며, 새로운 이상반응 양상은 나타나지 않았다는 것이 연구진의 설명이다.
이에 연구진은 이러한 연구결과가 면역항암요법에 실패한 전이성 요로상피세포암 환자에서 트로델비 단독요법을 더 평가할 것을 지지한다고 의미를 부여했다.
아울러 현재 백금 및 면역항암요법 후 질병이 진행한 요로상피세포암 환자에서 의사가 선택한 단일 항암화학요법과 트로델비를 비교하는 3상 임상 TROPiCS-04 연구가 진행되고 있다고 덧붙였다.


