[의약뉴스] 로슈의 면역관문억제제 티쎈트릭(성분명 아테졸리주맙)과 혈관신생억제제 아바스틴(성분명 베바시주맙)이 간세포암에 이어 담도암에서도 시너지를 확인했다.
기존의 항암화학요법에 티쎈트릭만 추가하는 것보다 아바스틴까지 추가하면 임상적 결과를 더 개선할 수 있다는 것.
다만 통계적으로 의미있는 차이는 보여주지 못해 기존의 표준요법을 바꾸지는 못한다는 지적도 나왔다.
20일(현지시간) 미국임상종양학회 소화기암 심포지엄(ASCO GI 2023)에서는 담도암환자를 대상으로 진행하고 있는 무작위 배정, 이중맹검, 임상 3상 IMbrave151 연구의 중간 분석 결과가 발표됐다.
이 연구는 이전 치료 경험이 없는 진행성 담도암 환자의 1차 치료요법으로 티쎈트릭과 항암화학요법(젬시타빈+시스플라틴) 병용요법에 아바스틴 또는 위약을 추가, 안전성과 유효성을 평가하고 있다.
연구의 1차 평가변수는 무진행생존율(Progression-Free Survival, PFS), 2차 평가변수는 전체생존율(Overall Survival, OS), 객관적반응률(Objective Response Rate, ORR), 반응지속기간(Duration or Response, DoR), 질병조절률(Disease Control Rate, DCR), 안전성, 환자가 보고한 삶의 질 등으로 정의했다.
이와 함께 탐색적 평가변수로 6개월 무진행생존율, 바이오마커 환자가 보고한 이상반응 등을 분석하도록 했다.
연구에 참여한 환자들은 모두 8주기 동안 젬시타빈과 시스플라틴 병용요법을 투약했으며, 한 그룹은 추가로 티쎈트릭과 아바스틴을, 다른 그룹은 티쎈트릭과 위약을 투약했다.
두 그룹의 환자들은 질병이 진행하거나 독성을 견딜 수 없거나 임상적 이득이 없다고 판단될 때까지 치료를 이어갔으며, 교차 투약(Crossover)은 허용하지 않았다.
연구에는 티쎈트릭+아바스틴 병용요법군에 79명, 티쎈트릭 단독요법(티쎈트릭+위약)군에 83명 등 162명을 대상으로 진행됐다.
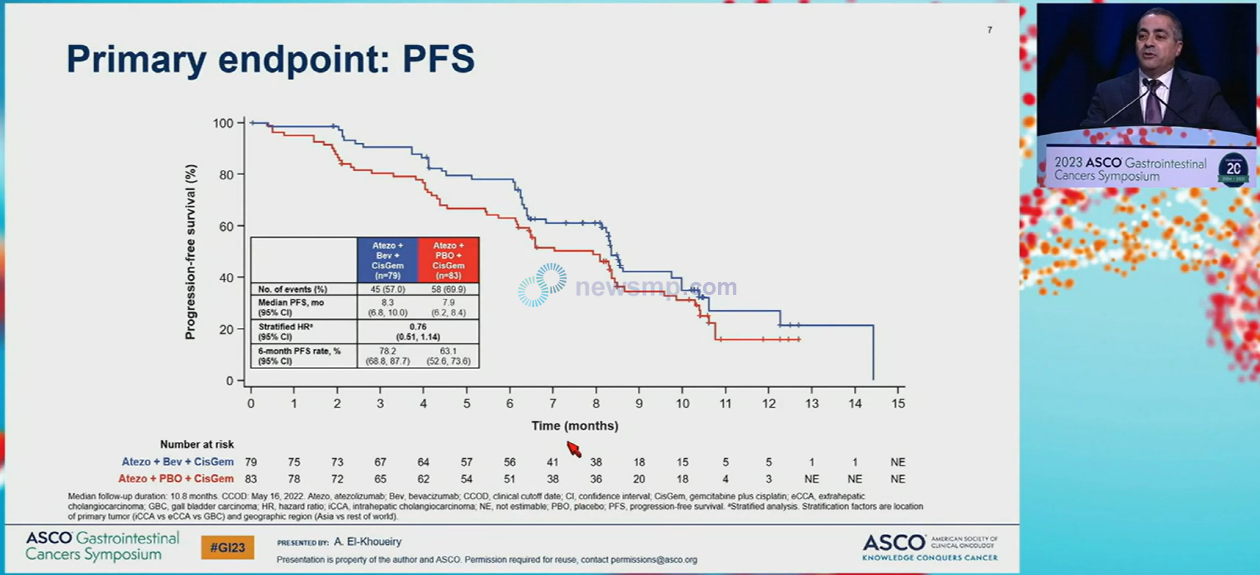
이번에 발표된 중간 분석의 중앙 추적관찰 기간은 10.8개월로, 병용요법군의 무진행생존기간 중앙값이 8.3개월, 위약군은 7.9개월로 병용요법의 질병 진행 또는 사망의 위험이 24% 더 낮은 경향을 보였다.(HR=0.76, 95% CI 0.61-1.14) 6개월 무진행 생존율은 78.2%와 63.1%로 집계됐다.
객관적반응률은 양군 모두 완전 반응(Complete Response, CR) 1명을 포함, 병용요법이 24.1%, 단독요법군이 25.3%로 거의 차이가 없었고, 질병조절률 또한 78.5%와 75.9%로 큰 차이가 없었다.
그러나 반응 지속기간 단독요법이 5.8개월에 그친 반면, 병용요법은 중앙값에 이르지 않았고, 6개월 무사건비율(event free rate)은 88.5%와 47.4%로 병용요법에서 반응이 소실될 위험이 78% 더 낮았다.(HR=0.22, 95% CI 0.07-0.73)
전체생존율 역시 단독요법군은 11.4개월로 집계된 반면, 병용요법군은 중앙값에 이르지 않았으며, 6개월 전체생존율은 92.0%와 80.5%로 병용요법군의 사망 위함이 26% 더 낮은 경향을 보였다.(HR=0.74, 95% CI 0.43-1.27)
특히 병용요법군의 이득은 반응이 나타난 환자에서 더 큰 차이를 보였다.
완전반응 또는 부분반응(Partial Response, PR)을 보인 환자에서 단독요법군의 무진행생존기간 중앙값은 8.3개월로 집계됐으나 병용요법군은 중앙값에 이르지 않아 병용요법의 질병 진행 또는 사망의 위험이 49% 더 낮은 경향을 보였다.(HR=0.51, 95% CI 0.18-1.49)
이와는 달리 안전병변(Stable Disease, SD)의 환자에서는 단독요법군의 무진행생존기간 중앙값이 8.4개월, 병용요법군은 8.3개월로, 양군간 차이가 없었다.(HR=1.00, 95% CI 0.59-1.71)
안전성에 있어 티쎈트릭과 아바스틴 병용요법은 관리 가능한 수준이었고, 아바스틴 추가로 발생한 독성은 미미했다.
티쎈트릭과 아바스틴 병용요법의 6개월차 무진행생존율과 전체생존율이 보다 높은 것은 특정 환자에서 임상적 이득이 있을 수 있음을 의미하며, 이에 바이오마커에 대한 연구를 진행하고 있다는 것이 연구진의 설명이다.
그러나 연구진의 긍정적인 평가와는 달리 메모리얼 슬론 케터링 암센터 이메인 엘 디카 교수는 이 연구 결과를 평가하면서 결과적으로 이 연구에서 병용요법이 무진행생존율이나 전체생존율, 반응률에서 차이를 보여주지 못했다고 지적했다.
환자수가 적어 통계적인 힘도 약하고, 양군 모두 기존의 대조군과 비교하기 어렵다는 평가다.
이어 담도암과 관련한 다양한 연구 결과들을 열거하면서, 더하는 것이 언제나 더 좋은 결과를 가져오는 것은 아니라고 강조했다.
이에 젬시타빈과 시스플라틴, 임핀지(성분명 더발루맙, 아스트라제네카) 병용요법이 여전히 담도암 1차 치료의 표준요법이라고 덧붙였다.


