항PD-(L)1 면역항암제 바벤시오(성분명 바벤시오, 머크)와 옵디보(성분명 니볼루맙, BMSㆍ오노)가 두경부암 임상에서 연이어 고배를 마셨다.
기존 표준치료와 비교해 무진행 생존기간(Progression-Free Survival, PFS)을 개선하는 데에는 성공했으나 사전에 설정한 유효성 범주에는 진입하지 못했다는 것이 연구진의 설명이다.
21일, 유럽종양학회 연례학술회의(ESMO 2021)에서는 국소 진행성 두경부암 환자를 대상으로 바벤시오와 상피세포성장인자수용체(EGFR) 억제제 얼비툭스(성분명 세툭시맙, 머크) 병용요법의 가능성을 평가한 GORTEC-REACH 3상 임상 결과가 공개됐다.

이 연구는 수술을 받지 않은 3, 4A, 4B기 국소 진행성 편평세포 두경부암 환자를 시스플라틴 적합 환자와 부적합 환자 코호트로 구분, 이들을 다시 각각 표준요법(방사선+시스플라틴 또는 얼비툭스)군과 방사선요법+얼비툭스+바벤시오 병용요법 이후 바벤시오 유지요법군(이하 실험군)으로 배정해 안전성과 유효성을 비교했다.
이 가운데 시스플라틴 부적합 환자군에서 2년 시점의 무진행 생존율은(중앙 추적관찰 21.3개월) 실험군이 44%로 표준요법(방사선요법+얼비툭스 병용)군의 31%와 비교해 질병 진행 또는 사망의 위험이 16% 더 낮았으나(HR=0.84, P=0.14) 통계적 유의성은 없었으며, 사전에 정의한 유효성 범주(HR=0.62)에 들어서지도 못했다.
뿐만 아니라 시스플라틴 적합 환자(방사요법+시스플라틴)에서는 1년 시점 무진행 생존율이 표준요법군은 73%, 실험군이 64%로 오히려 표준요법군의 질병 진행 또는 사망의 위험이 더 낮아 열등성 범주에 들어갔다.
이어 발표된 CheckMate 651 임상에서도 아쉬운 성적이 나왔다.
CheckMate 651은 재발/전이성 편평세포 두경부암 환자를 대상으로 1차 치료제로 옵디보(2주 간격)+여보이(성분명 이필리무맙, BMS, 6주 간격) 병용요법(최대 2년)을 표준요법인 EXTREAM 요법(얼비툭스+시스플라틴/카보플라틴+5-FU 6주기 후 얼비투스 유지요법)과 비교했다.
이 연구는 환자들을 PD-L1 발현율(CPS 기준)에 따라 구분, 전체 무작위 배정 환자군에서의 무진행 생존율과 CPS 20 이상 환자군에서의 전체 생존율(Overall Survival, OS)을 1차 평가변수로 설정했다.
다만, 둘 모두 유효성 범주(log-rank test α=0.025) 안에 들어서면 1차 평가변수를 충족하는 것으로 정의하되, 둘 중 하나만 충족하는 경우에는 CPS 1이상에서의 전체 생존율을 추가로 분석하거나, 혹은 유효성 범주를 α=0.05로 확대해 재평가하도록 했다.
그러나 연구 결과 전체 무작위 배정 환자와 CP 20이상 모두 유효성 평가범주에 들어서지 못해 1차 평가변수를 충족하지 못했다.
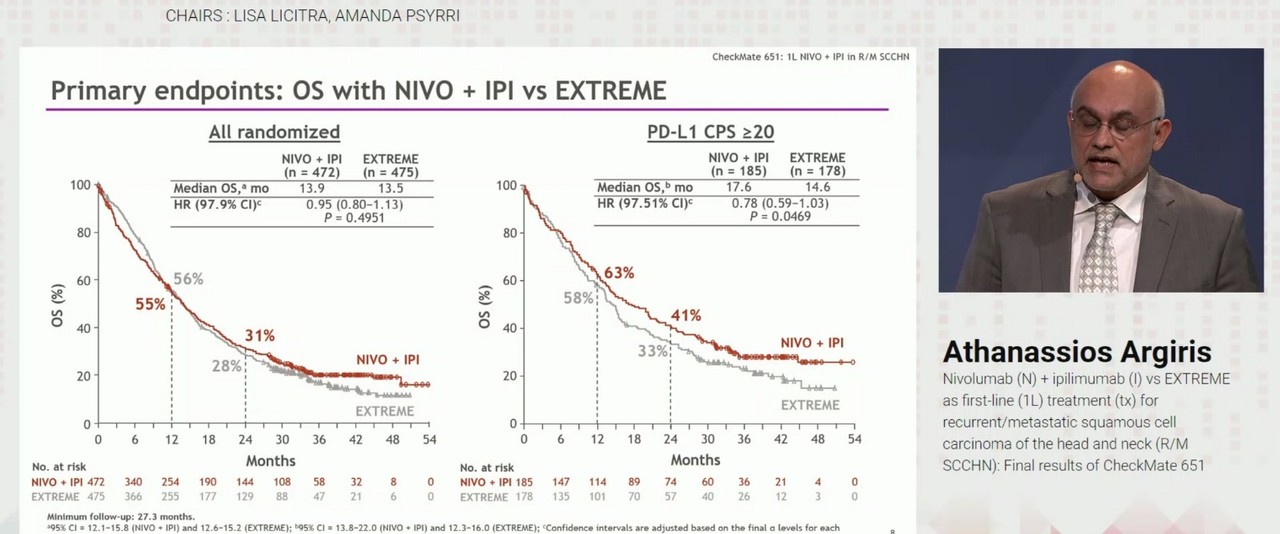
먼저 전체 무작위 배정 환자에서는 옵디보+여보이 병용군의 전체 생존기간 중앙값이 13.9개월, 표준요법군은 13.5개월로 상대위험비(Hazard Ratio, HR)는 0.95, P 값은 0.4951로 집계됐다.
CPS 20 이상인 환자에서는 옵디보+여보이군의 전체 생존기간 중앙값이 17.6개월, 표준요법군은 14.6개월로 상대위험비가 0.78, P 값은 0.0469로 집계됐다.
이처럼 1차 목표 달성에 실패한 가운데, 전체 환자에서 또 다른 유효성 평가지표 중 무진행 생존기간 중앙값은 옵디보+여보이 병용군이 3.3개월에 그쳐 표준요법군 6.7개월의 절반에 그쳤고, 객관적 반응률(Objective Response Rate, ORR)도 24%와 37%로 표준요법이 더 높았다.
다만, 반응 지속기간(Duration of Response, DoR)은 16.6개월과 5.9개월로, 옵디보+여보이군이 3배 가까이 길었다.
이 같은 양상은 CPS 20 이상인 환자군은 물론 CPS 1이상인 환자군에서도 동일하게 나타났다.
CPS 20 이상인 환자들을 대상으로 분석한 질병 악화까지의 시간이나 삶의질 평가에서도 옵디보+여보이군이 더 좋은 결과를 얻었다.
비록 1차 평가변수가 사전에 설정한 유효성 범주에 들어서지는 못했지만, CPD 1이상인 환자나 20 이상인 환자에서 옵디보+여보이 군의 임상적 이점은 보여주었다는 것이 연구진의 평가다.


