지난 5월 한 달 동안 식품의약품안전처의 승인을 받은 임상시험이 총 54건으로 지난해 5월 52건 대비 3.8% 증가했다. 반면 전월인 4월 59건과 비교했을 때에는 8.5% 감소했다.
올해 임상시험 승인 건수를 월별로 살펴보면 1월 57건에서 2월 43건으로 줄었다가 3월에는 76건까지 급증했다. 이어 4월부터는 다시 감소세로 돌아섰으나, 전년 대비로는 비슷하거나 높은 수준을 유지했다.
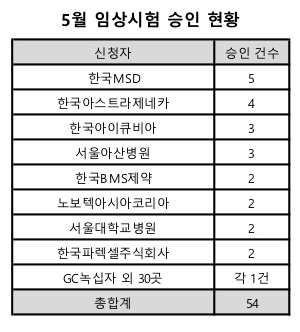
신청자별로 살펴보면 한국MSD가 5건으로 가장 많았으며, 한국아스트라제네카가 4건, 서울아산병원과 한국아이큐비아가 각 3건, 한국BMS제약과 노보텍아시아코리아, 서울대학교병원, 한국파렉셀이 각 2건, 녹십자 등 총 31곳이 각 1건씩 승인 받았다.
국내 주요 제약사의 임상시험 승인 현황을 날짜별로 살펴보면 5월 9일에는 대화제약과 신일제약이 시타글립틴 성분 제제의 임상1상을 각각 승인 받았고, 20일에는 한미약품이 HCP1704의 임상1상을, 21일에는 GC녹십자가 자가면역뇌염환자에 대한 아이비-글로불린에스엔주 10%의 임상2상을 승인 받았다.
24일에는 경동제약이 KD5001의 임상1상을, 제넥신은 교모세포종 환자를 대상으로 한 GX-I7의 임상1/2상을, 28일에는 보령제약이 피마사르탄·암로디핀·히드로클로로티아지드 성분인 FAH정의 임상3상을 승인 받은 것으로 조사됐다.
30일에는 대웅제약이 SGLT-2억제제 계열 당뇨병 치료제 DWP16001의 임상2상을 승인 받았고, 31일에는 메디포스트가 SMUP-IA-01의 임상1상을 승인 받았다.
한편 임상시험 단계별로 살펴보면 3상이 16건으로 가장 많았으며, 1상이 13건, 2상 11건, 연구자임상시험 8건, 1/2상 3건, 2a상 2건, 1b상 1건씩이었다.


