잠재가치가 높은 의료기술의 빠른 시장 진입을 돕기 위한 제도가 도입돼 내일(15일)부터 운영된다.
보건복지부는 혁신의료기술 별도평가트랙 도입, 신의료기술 평가기간 단축을 골자로 하는 ‘신의료기술평가에 관한 규칙’ 개정안을 15일 공포·시행할 예정이다.
현행 제도 하에서 새로운 의료기술은 신의료기술평가를 통해 안전성과 유효성 검증을 마친 후에 현장에서 사용할 수 있다. 이러한 안전성·유효성 평가는 출판된 문헌을 근거로 이뤄져왔다.
하지만 이 같은 평가체계는 문헌근거를 쌓을 시간적 여유가 부족한 혁신의료기술에는 불리하다는 지적이 많았다. 실제로 로봇, 3D 프린팅 융합 의료기술의 신의료기술평가 탈락률(2016∼2018년 9월)은 82%에 달한다.
이에 시행을 앞두고 있는 개정 법령에서는 ‘첨단기술이 융합된 의료기술’, ‘암, 심장질환 등 중증 질환을 치료하거나 환자의 만족도를 증진시키는 의료기술’은 현행 신의료기술평가가 아닌 별도평가트랙을 활용할 수 있도록 했다.
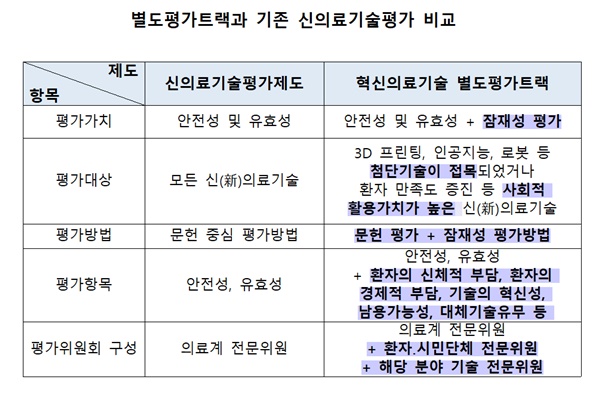
‘혁신의료기술 별도평가트랙’에서는 문헌 중심 평가와 더불어 새로 개발된 의료기술의 잠재성 평가까지 진행해 환자의 삶을 획기적으로 개선하거나 환자의 비용 부담을 줄여주는 등 높은 잠재성을 가졌을 경우 조기 시장 진입을 허용한다.
다만, 혁신의료기술이라 하더라도 사람의 인체 조직 내부에 행해지는 의료행위(침습적 의료행위)로 환자의 부담이 큰 의료기술에 대해서는 문헌을 통한 엄격한 안전성 검증을 실시한다.
‘혁신의료기술 별도평가트랙’을 통해 의료현장에 도입된 혁신의료기술은 의료현장에서 활용된 결과를 바탕으로 3~5년 후 재평가를 받아야 한다.
재평가를 위해 혁신의료기술을 개발한 의료기기 업체는 이를 사용하는 의료기관, 실시 의사 등의 자료를 한국보건의료연구원(NECA)에 제출해야 한다. 자료를 허위로 제출하거나 허용된 의료기관 이외에서 의료기술을 사용할 경우 혁신의료기술 사용이 중단될 수 있다.
한편, 개정 법령이 시행되면 현행 신의료기술평가 기간도 30일(최대 280→250일) 단축된다.
당국은 전문가 서면 자문을 통해 신의료기술평가 대상 여부를 판단했던 절차를 내부 평가위원으로 대체하기로 하고 이를 개정 법령에 반영했다.
평가절차가 2단계에서 1단계로 줄어들면 외부 전문가 탐색과 구성 등에 필요했던 시간을 절약할 수 있다.


