10월에 이어 11월에도 70건 이상의 임상시험이 승인된 것으로 나타났다.
식품의약품안전처가 11월 한 달 동안 승인한 임상시험계획은 총 73건으로 지난 10월 74건 대비 1.4% 줄었으나, 지난해 11월 50건 대비 46.0% 증가했다.
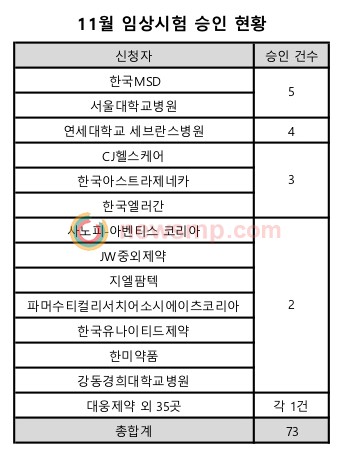
신청자별로 살펴보면 서울대학교병원과 한국MSD가 각 5건으로 가장 많았으며, 연세대학교 세브란스병원이 4건, CJ헬스케어와 한국아스트라제네카, 한국엘러간이 각 3건, 사노피-아벤티스코리아와 JW중외제약, 지엘팜텍, 파머수티컬리서치어소시에이츠코리아, 한국유나이티드제약, 한미약품, 강동경희대학교병원이 각 2건, 대웅제약 등 총 36곳이 각 1건씩 승인 받았다.
국내 주요 제약사의 임상시험 승인 현황을 살펴보면 CJ헬스케어는 테고프라잔과 메트로니다졸, 테트라사이클린, 비스무트의 경구 반복 투여 시 약동학적 상호작용을 평가하기 위한 임상1상 시험과 테고프라잔과 클로피도그렐 병용 투여 시 테고프라잔이 클로피도그렐의 약력학에 미치는 영향을 CYP2C19 유전형에 따라 평가하기 위한 임상1상 시험, CJ-14199의 안전성·내약성 및 약동학·약력학적 특성을 평가하기 위한 임상1상 시험을 승인 받았다.
JW중외제약은 JW1601 경구 투여 시 안전성·내약성 및 약동학·약력학적 특성 평가를 위한 임상1상과 통풍 환자를 대상으로 URC102의 유효성 및 안전성을 평가하기 위한 임상2b상을, 한국유나이티드제약은 UI022/UI023의 유효성과 안전성을 평가하기 위한 임상3상과 UIC201806·UIC201602를 병용 투여 또는 UI018 단독 경구 투여 후 안전성과 약동학적 특성을 비교 평가하기 위한 임상1상을 각각 승인 받은 것으로 조사됐다.
아울러 한미약품은 재발성 또는 불응성 급성 골수성백혈병 환자에서 HM43239의 안전성, 내약성, 약동학, 약력학에 대한 임상1/2상 및 HIP1801의 약동학적 특성 및 안전성·내약성을 평가하기 위한 임상1상을 승인 받았다.
이밖에 경동제약이 다파진정의 임상1상을, 휴젤은 BMT101의 임상2a상을, 안국약품이 SDR18-P3의 임상3상을, 동화약품은 자보란테의 임상3상을, 셀트리온이 CT-P16의 임상3상을, 한림제약은 HL237의 임상1상을, 일동제약이 LB80380의 임상4상을, 신신제약은 UI(PT)620의 임상1상을, 대웅제약이 DWP14012의 임상3상을, 제넥신이 GX-I7의 임상1/2a상을 각각 승인 받은 것으로 확인됐다.
한편 단계별로는 임상3상이 22건으로 가장 많았으며 1상과 연구자임상이 각 14건, 1/2상과 2상이 각 5건, 2b상 3건, 1/2a상과 1b상, 4상이 각 2건, 2a상과 3/4상, 3b상, 연장임상시험이 각 1건씩이었다.


